Modelo Cuantico
Quienes sentaron las bases del nuevo modelo mecanico cúantico fueron tres científicos:
1° En 1924, Louis de Broglie, postuló que los electrones tenían un comportamiento dual de onda y partícula. Cualquier partícula que tiene masa y que se mueve a cierta velocidad, también se comporta como onda.
2° En 1927, Werner Heisenberg, sugiere que es imposible conocer con exactitud la posición, el momento y la energía de un electrón. A esto se le llama "principio de incertidumbre"
3° En 1927, Erwin Schrödinger, establece una ecuación matemática que al ser resuelta permite obtener una función de onda (psi cuadrado) llamada orbital. Esta describe probabilisticamente el comportamiento de un electrón en el átomo. Esta función es llamada densidad electrónica e indica la probabilidad de encontrar un electrón cerca del núcleo. La probabilidad es mayor mientras más cercana al núcleo y menor si nos alejamos del núcleo. Con esta teoría de Schrödinger queda establecido que los electrones no giran en orbitas alrededor del núcleo como el modelo de Bohr, sino en volumenes alrrededor del núcleo.
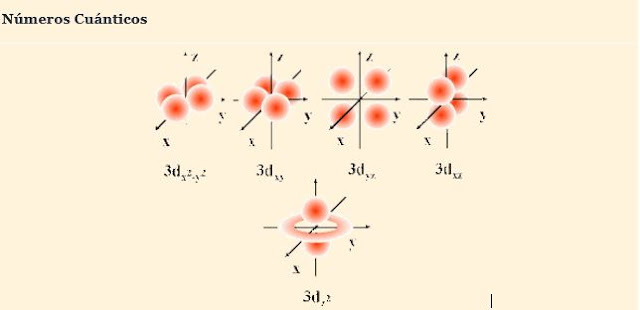 |
| Imagen tomada de: http://quimica1m.blogspot.mx/p/configuracion-electronica.html |
La distribución de los electrones alrededor del núcleo obedece a una serie de reglas que se traducen en un modelo matemático que reconoce 4 números cuánticos:
1. Número cuántico principal (n): corresponde a los niveles de energía. Estos niveles aumentan de tamaño a medida que nos alejamos del núcleo. Posee valores n=1, 2, 3, 4, 5, 6,...
2. Número cuántico secundario (l): representa la existencia de subniveles de energía dentro de cada nivel. Se calculan considerando l = 0, 1, 2, 3, 4
Así, para n=1...l =0 ( "s" )
para n=2 .........l = 0, 1 ( "s", "p" )
para n=3 .........l = 0, 1, 2 ( "s", "p", "d" )
para n=4 .........l = 0, 1, 2, 3, 4 ("s", "p", "d", "f" )
3. Número magnético (m): representa la orientación de los orbitales y se calcula m=+/- l
si l = 0, m=0 es decir 1 solo tipo de orbital s
si l = 1, m =-1, 0, +1 es decir 3 tipos de suborbitales p (px, py y pz)
si l = 2, m = -2, -1, 0, +1, +2 es decir 5 tipos de suborbitales d (du, dv, dx, dy, dz)
si l = 3, m = -3, -2, -1, 0, +1, +2, +3 es decir 7 tipos de suborbitales f (fs, ft, fu, fv, fx, fy y fz)
4. Número de spin (s): indica la cantidad de electrones presentes en un orbital y el tipo de giro de los electrones, habiendo dos tipos +1/2 y -1/2. En cada tipo de suborbital cabe máximo 2 electrones y estos deben tener spines o girpos opuestos.
Bibliografía;
La información fue tomada el día: 28/06/2017
De las páginas:

Comentarios
Publicar un comentario